Werking van antibiotica
Hoe werken antibiotica tegen bacteriën? (en niet tegen de mens die ze slikt?)
Ze werken altijd op een specifiek aangrijpingspunt ,dus op iets dat een bacterie (prokaryoot) wel heeft en een gastheer (eukaryoot) niet,en zijn daar door selectief giftig (toxisch) en wel bij de volgende processen:
- remming celwandsynthese van de bacterie.
- remming eiwitsynthese,(dat deel wat bacteriespecifiek is)
- beschadigen van de buitenste celmembraan (bij gramnegatieve bacterien)
- remming van de nucleïnezuursynthese (dat deel dat bacteriespecifiek is)
- aangrijpen op de specifieke bacteriestofwisseling
Antibiotica werken vooral goed als geneesmiddel tegen infectieziektes als de bacterie actief is.
Antibiotica werken niet tegen virussen en dus ook niet tegen griep en virale keelontsteking.
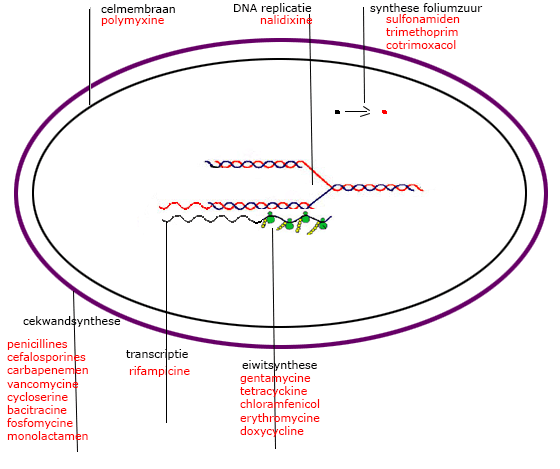
Hierboven de zwakke plekken van de bacterie, lees hier meer over de werking.
De remming van de celwandsynthese
Zoals je misschien nog weet bestaat de celwand van bacteriën uit peptidoglycaan (mucopeptide), zie celwand en onderstaand plaatje
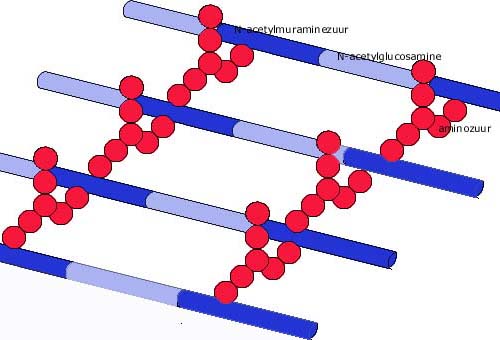
Andere organismen bezitten deze structuur niet.
Penicilline en nog enkele andere antibiotica (cephalosporines) remmen de synthese van peptidoglycaan, ze verstoren de vorming van de (rood in plaatje) eiwit dwarsverbindingen tussen de aminosuikers NAG en NAM,, het gevolg is een sterk verzwakte celwand waardoor de cel lyseert. Het is een bactericide middel. Omdat alleen de synthese wordt verstoord werkt penicilline uitsluitend op groeiende cellen. De celwanden verzwakken en de cel knapt: zie video
Penicilline bestaat in verschillende nauw aan elkaar verwante vormen.
Het prototype is penicilline G. Het heeft een smal maar nuttig werkingsspectrum en is vaak de eerste keus tegen de meeste staphylococcen, streptococcen, en enkele spirochaeten.
Hoewel veel gebruikt zijn er ook enkele nadelen:
Nadelen
Het antibioticum kan slecht tegen een lage pH, een nadeel voor oraal (pilletje) gebruik en kan slecht tegen penicillinase een enzym gevormd door resistente bacteriestammen.
Penicillinase verbreekt de lactam ring van het penicillinemolecuul reden om penicillinase ook wel ß-lactamase te noemen.
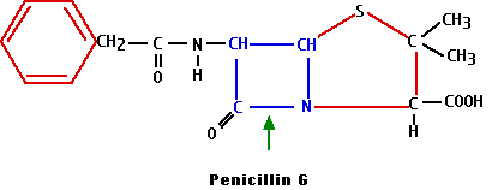
Verbeterde penicillinemoleculen
Om deze nadelen op te heffen is men gaan sleutelen aan het penicillinemolecuul (tijdens de productie) door het halverwege laten stoppen van de penicillinesynthese door de schimmel en vervolgens de kern (ß-lactamring= werkzaam gedeelte, de vierkante ring in bovenstaande structuurformule) van het molecuul te gebruiken voor verdere aanbouw van zijketens met als doel deze ongevoelig te maken voor zuur en penicillinase.
Ook kan men van het al complete molecuul de zijketen verwijderen en vervangen door een andere keten.
In beide gevallen is er sprake van een gedeeltelijke aanmaak door de schimmel een een gedeeltelijk chemisch proces, vandaar de naam semi-synthetische of halfsynthetische penicillinen.
Steeds weer nieuwe antibiotica: waarom?
Methicilline was een van de eerste halfsynthetische penicillinen, bedoeld om de penicillinasewerking van de resistente stammen te weerstaan (door de andere ruimtelijke structuur paste het niet meer in het penicillinasemolecuul van de bacterie) werd zeer veel gebruikt. Echter vele bacteriesoorten ontwikkelden opnieuw resistente stammen , nu tegen deze stof, zodat als opvolger oxacilline is ontwikkeld. Ook kan men semi-synthetische penicillinen ontwikkelen met een breder werkingsspectrum, zoals ampicilline en amoxicilline.. Toen de resistentie tegen deze stoffen gebruikelijk werd werden de carboxypenicillinen ontwikkeld Zo gaat de ontwikkeling steeds verder: men ontwikkelt een nieuw antibioticum, de bacterie ontwikkelt een resistentie en men zal weer een nieuw antibioticum moeten ontwikkelen. Behalve voor penicilline geldt deze resistentieproblematiek ook voor alle andere antibiotica (met de andere werkingsmechanismen die hieronder worden besproken)
Andere celwandsynthese remmers zijn: Vancomycine en bacitracine deze werken op de vorming van de lange ketens van aminosuikers NAG en NAM (de blauwe staven in het plaatje), en de Carbapenems . In Nederland worden de laatste stoffen zeer terughoudend voorgeschreven omdat ze als laatste redmiddel gebruikt worden als andere antibiotica niet helpen tegen een bepaalde bacterie. Ze worden alleen in het ziekenhuis gebruikt.
Het op slot zetten van de celwandgroei
In 2020 zijn er antibiotica ontdekt die ook op de celwand werken maar dan door precies het tegenovergestelde te doen: ze verhinderen dat de wand wordt afgebroken waardoor verder groei en celdeling onmogelijk is. De celinhoud zit als het ware gevangen in de te kleine celwand waardoor de cel niet groter kan worden en zich niet kan delen. En zonder deling geen groei!
De remming van de eiwitsynthese
Omdat de eiwitsynthese zowel bij eukaryote als prokaryote cellen voorkomt lijkt het een ongeschikt doelwit voor een selectief giftige stof.
Er is echter een verschil: de structuur van de ribosomen.
Eukaryote cellen hebben 80S ribosomen, prokaryote cellen 70S ribosomen. Hierdoor kunnen antibiotica toch selectief de eiwitsynthese van de prokaryote cel verstoren.
De mitochondriën van de eukaryote cel bevatten echter ook 70S ribosomen: oorzaak van de bijwerkingen die deze antibiotica kunnen vertonen. Bekende voorbeelden zijn streptomycine, erythromycine, chlooramfenicol en tetracycline.
Beschadiging van de celmembraan
De polypeptideantibiotica, veranderen de doorlaatbaarheid van de membraan, waardoor belangrijke stofwisselingsproducten uit de cel lekken. Zo maakt polymyxine B door zijn hechting aan de fosfolipiden de celmembraan kapot.
Het middel is bactericide. het werkt uitsluitend tegen gram-negatieve cellen.
Omdat het tegen de celmembraan werkt is het ook giftig voor de mens het wordt daarom slechts in speciale gevallen gebruikt. (zalven, sterilisatie van het maag-darmkanaal: mogelijk omdat de stof niet geresorbeerd wordt).
In de analytische microbiologie is de stof geschikt voor de bereiding van selectieve voedingsmedia.
De remming van de nucleinezuursynthese
Een aantal antibiotica interfereren met de DNA-replicatie en transcriptie in micro-organismen.
De meeste stoffen met deze werking zijn ook zeer giftig voor de gastheer, enkele niet zoals rifampicine dat zich bindt aan het enzym RNA-polymerase (zorgt voor transcriptie) van bacteriën en virussen.
Remming van de stofwisseling.
Als een antibioticum in staat is de synthese van een voor de bacterie (niet voor de gastheer!) belangrijk stofwisselingsproduct te verhinderen, dan zal de bacterie niet meer kunnen groeien. Hieronder wordt besproken hoe dat mogelijk is:
Hoe fop je een enzym?(Competitieve remstoffen)
Meestal wordt de synthese geblokkeerd doordat het antibioticum zoveel op een substraat lijkt dat het de plaats van dit substraat gaat innemen op het enzym dat verantwoordelijk is voor de synthese van de onmisbare stof.: competitieve remming.
Een heel bekend voorbeeld is de synthese van foliumzuur. Foliumzuur is onmisbaar voor de aanmaak van de basen in het RNA en DNA en vele aminozuren.
Zoogdieren nemen dit foliumzuur op met het voedsel, micro-organismen kunnen dit niet door de celmembraan opnemen, hetgeen de selectieve werking van sulfanilamide verklaart.
Para-amino-benzoezuur moet door een enzym omgezet worden in dit foliumzuur.
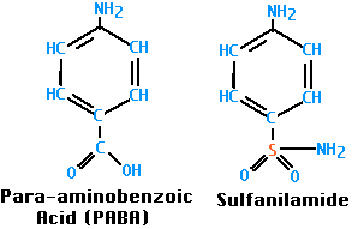
Echter sulfanilamide het door Ehrlich ontdekte antibioticum lijkt zeer veel op para-amino-benzoezuur , gaat op het enzym zitten, verhindert zo de omzetting in foliumzuur en stopt de groei van het micro-organisme.
Zulke stoffen die de stofwisseling verstoren (blokkeren) worden ook wel antimetabolieten genoemd.
Het combineren van antimicrobiële geneesmiddelen
Soms dient men twee antibiotica tegelijk toe; in spoedgevallen waarbij de ziekteverwekker niet bekend is, bij menginfecties van bacteriën die verschillen in gevoeligheid, maar ook om een betere werkzaamheid te krijgen dan met één middel het geval is. Dit verschijnsel wordt synergisme genoemd, zo wordt bij een ernstige streptococceninfectie wel een combinatie van ampicilline en gentamycine gebruikt. Ampicilline verzwakt de wand van de streptococ zodat het gentamycine gemakkelijker toegang krijgt tot de cel.
Het tegenovergestelde ongewenste effect dat twee antibiotica elkaar in werking verzwakken heet antagonisme, zo kan de combinatie van een bacteriostatisch middel met een bactericide middel problemen opleveren; het bacteriostatische middel bijvoorbeeld chlooramfenicol legt de groei van de bacterie plat waardoor een bactericide middel dat de bouw van de celwand verstoort zijn werk niet kan doen.
Indeling van antibiotica in een aantal hoofdgroepen |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
De ene bacterie is de andere niet
Kijken we weer naar de antibiotica dan zijn er ook onderlinge verschillen. Sommige antibiotica hebben een smal werkingsspectrum, dat wil zeggen dat ze tegen een beperkt aantal groepen van bacteriën werkzaam zijn. Zo werkt penicilline tegen grampositieve bacteriën en slecht(s) tegen enkele gramnegatieve bacteriën. Antibiotica die tegen een groot aantal zowel gramnegatieve als grampositieve bacteriegroepen werken noemt men breed-spectrumantibiotica,
Waarom niet?
Een verklaring voor deze selectieve toxiciteit is gelegen in het feit dat gramnegatieve cellen een buitenmembraan om de celwand hebben, hierin bevinden zich poriën, kleine met water gevulde kanaaltjes. Stoffen die deze kanaaltjes kunnen passeren moeten niet al te groot zijn en bij voorkeur hydrofiel. Erg grote moleculen en stoffen die lipofiel zijn komen niet gemakkelijk een gramnegatieve cel binnen.
Waarom niet alleen breedspectrum antibiotica gebruiken?
Omdat de identiteit van een ziekteverwekker niet altijd direct bekend is lijkt een breed-spectrumantibioticum op het eerste gezicht het meest aantrekkelijk doordat een tijdrovende identificatie niet nodig is en men direct met de behandeling kan beginnen.
Er zijn echter twee nadelen:
Het eerste nadeel is echter dat de normale (darmflora) van de patiënt door een breed-spectrumantibioticum vernietigd wordt. Deze flora is nuttig omdat deze een competitie voert met eventueel binnendringende pathogene micro-organismen. Deze vorm van natuurlijke afweer gaat zo verloren.
Ook kunnen overlevende micro-organismen van de flora van de patiënt zich gaan ontwikkelen en pathogeen worden opportunistiche pathogenen. Een bekend voorbeeld is de groei van de gist Candida albicans.
Bactericide stoffen
Een stof kan bactericide zijn , dan doodt het bacteriën ( denk aan insecticide)
Bacteriostatische stoffen
Bacteriostatische stoffen remmen bacteriën, er vindt geen toename plaats (denk aan thermostaat) Omdat groei wordt voorkomen kan de afweer de gastheer de bacteriën bestrijden.
Waarom werken antibiotica alleen tegen bacteriën?
De oorzaak is dat er tussen prokaryote en eukaryote cellen veel verschillen zijn: de aanwezigheid/ afwezigheid van een celwand, de bouw van de ribosomen, en details in de stofwisseling.
Schimmels, protozoën en wormen lijken te veel op ons!
Een probleem ontstaat als de pathogeen eukaryoot is: schimmels, protozoën en wormen. Deze laatste lijken door hun eukaryote cel zo veel op de te behandelen gastheer dat er veel minder aangrijpingspunten voor een selectief remmende of dodende stof zijn, er zijn dan ook minder van dergelijke geneesmiddelen.
Een anti-schimmelstof
Er zijn ook antibiotica die (tamelijk selectief) tegen schimmels werken dankzij het feit dat ze zich hechten aan de sterolen die in de schimmelcelmembraan aanwezig zijn, waardoor deze kapot gaat.
Omdat bacteriën geen sterolen bevatten werken deze stoffen niet tegen bacteriën
De zoogdiercel bevat echter wel sterolen in zijn celmembraan, zodat de antibiotica giftig kunnen zijn voor de gastheer.
Gelukkig bevat de zoogdiercel voornamelijk het sterol cholesterol en de schimmelcel het sterol ergosterol in de celmembraan, zodat meestal de voordelen groter zijn dan de nadelen.
Voorbeeld van zo'n stof is nystatine (ook wel natamycine ) genoemd, veel gebruikt bij huidinfecties veroorzaakt door schimmels en in de kaasindustrie om beschimmelen van de kaaskorst te voorkomen.
En virussen maken gebruik van onze stofwisseling
Voor virussen is het nog moeilijker een selectief remmende stof te vinden omdat deze organismen in de gastheer gebruik maken van de stofwisseling en de organellen van de gastheer. Rem je het virus dan leg je ook de stofwisseling van de gastheer plat.
Antibiotica werken niet tegen virussen : dus
Bij verkoudheid en griep helpen antibiotica niet
[ Resistentie ]
[ antibiotica op het lab]
[ontdekking antibiotica]